-
우리 학교 박은덕 교수 연구팀이 바닷물과 태양광만을 이용해 부가가치가 높은 화합물과 청정 수소를 동시에 생산할 수 있는 친환경 시스템을 구현하는 데 성공했다.박은덕 교수(화학공학과·대학원 에너지시스템학과) 연구팀의 해당 연구는 ‘바닷물/클로로포름 전해질에서의 티타늄이 도핑된 산화철 광산화전극을 통한 탠덤 광전기화학적 sp3 탄소-수소 결합 염소화(Photoelectrochemical tandem chlorination of sp3 C–H bond in seawater/chloroform two-phase electrolyte system by Ti-doped Fe2O3 photoanode)’라는 제목으로 <미국화학회지(Journal of the American Chemical Society)> 6월호에 게재됐다. 박은덕 교수가 교신저자(위 사진 왼쪽)로, 아주대 채상윤 박사후 연구원(대학원 에너지시스템학과·차세대에너지과학연구소, 사진 가운데)과 아딜 메흐무드(Adeel Mehmood) 박사후 연구원(대학원 에너지시스템학과·나노정보기술융합연구소, 사진 오른쪽)이 제1저자로 참여했다.화학 산업에서는 고부가가치 화합물을 지속가능하고 친환경적인 방식으로 제조하는 기술의 개발이 점점 더 관심을 받고 있다. 석유화학이나 철강 산업에서 활용되는 다양한 화합물의 생산 과정에서 막대한 에너지가 소모되고, 이 과정에서 이산화탄소와 같은 온실가스나 기타 유해 물질이 배출되어 인체 건강과 환경에 부정적인 영향을 미치기 때문이다. 특히 화학 공정에서 핵심적으로 요구되는 탄소-수소 결합의 활성화 반응은 유해 가스나 대량의 유기용매 사용을 필요로 한다는 점에서 개선이 요구된다.이러한 한계를 극복하기 위한 대안으로 산업계와 학계에서 태양광과 같은 재생에너지를 활용한 화합물 제조 방식이 주목받고 있다. 광전기화학전지(PEC) 시스템을 활용하면 태양에너지를 화학에너지로 변환, 이를 통해 유기물의 탄소-수소 결합을 선택적으로 활성화하고 염소나 브롬 등 할로겐이 선택적으로 치환되어 정밀화학 제품이나 의약품 등의 원료로 사용이 가능한 고부가가치 화합물로 전환할 수 있으며, 동시에 수소도 생산할 수 있다. 이러한 반응의 효율을 높이기 위해서는 적절한 반도체 광전극과 그에 맞는 시스템의 개발이 꼭 필요하다.기존에 널리 활용되어 온 방안은 탄소-수소 결합의 할로겐화 반응을 이용하는 것으로, 반응물과 할로겐 원소가 하나의 전해질에 용해되어있는 시스템이다. 그러나 이 방안은 일반적으로 유독한 할로겐 가스를 외부에서 주입하거나 고가의 시약을 사용하는 방식이어서 안전성과 환경성, 비용 측면에서 한계를 갖는다.아주대 연구팀은 이러한 부분을 개선하기 위해 기존 연구에서 유독한 할로겐 가스를 직접 사용하지 않고, 전해질을 분리해 친환경적인 브롬화 이온으로부터 태양광을 이용해 반응에 필요한 브롬가스를 실시간으로 공급한 바 있다. 그러나 브롬화 이온 역시 자연에서 쉽게 구할 수 없다는 점이 해당 연구의 한계였다. 이에 아주대 연구팀은 추가 연구를 통해 산화철 광전극과 산성 바닷물 및 클로로포름 유기상으로 구성된 광전기화학전지–이중상 전해질 시스템을 설계했다.연구팀은 해당 시스템에서 바닷물에 풍부하게 함유된 염화 이온을 산화철 광전극이 태양광을 이용해 염소가스로 실시간 전환하고, 이를 염소화 반응에 활용하여 다양한 유기물의 탄소-수소 결합을 효과적으로 활성화해 염소화시키는 것을 확인했다. 산화철 전극은 바닷물에서도 95% 이상의 매우 높은 염소 생성 선택성을 보였다. 특히 이 시스템은 고가의 귀금속 촉매나 반도체 물질을 전혀 사용하지 않고, 자연에 풍부한 산화철 광전극과 바닷물을 직접 전해질로 활용, 별도의 정제 과정 없이 실시간으로 염소가스를 생성하고, 100% 위치 선택적 염소화 반응을 구현했다는 데 의의가 있다.박은덕 교수는 “이번 연구는 태양광과 자연 바닷물이라는 지속 가능한 자원을 활용하여, 환경친화적이고 안전한 유기합성 반응을 구현했다는 점에서 의미가 있다”라며 “태양광 기반의 유기화학 및 수소생산 융합 기술의 새로운 가능성을 보여주는 사례”라고 설명했다. 박 교수는 이어 “염소화 반응뿐 아니라 다양한 유기 기능화 반응으로 확장 가능하며, 해수 전기분해 기반의 탄소-수소 결합 선택적 활성화 기술로서 활용성이 매우 높다”라고 덧붙였다.이번 연구는 한국연구재단의 C1 가스 리파이너리 사업, G-램프 사업, 기초연구지원사업의 지원으로 수행됐다.태양광을 이용해 해수에서 수소와 고부가 화합물을 동시에 제조하는 모식도
-
211
- 작성자통합 관리자
- 작성일2025-06-12
- 1589
- 동영상동영상
-
아주대 장혜영 교수팀이 대표적 온실가스인 이산화탄소와 생분해성 플라스틱의 원료인 락타이드를 기반으로 한 고분자 합성법을 개발했다. 기존 플라스틱 생산에 활용되는 석유 기반 고분자를 친환경적 소재로 대체할 수 있는 가능성을 확인한 연구다.해당 연구는 ‘아연-갈산 촉매를 통한 구성 요소 및 구조 조절이 가능한 고성능 이산화탄소 기반 고분자 합성(Zn-gallate catalyzed synthesis of high performance CO2-polymers with tunable composition and architecture)’이라는 논문으로 화학 분야 국제 학술지인 <저널 오브 CO2 유틸라이제이션(Journal of CO2 Utilization)>에 5월 온라인 게재됐다.아주대 화학과 장혜영(위 사진 왼쪽)∙이인환(위 사진 오른쪽) 교수팀의 공동 연구 성과로, 대학원 에너지시스템학과 김재호(석사과정) 졸업생이 제1저자로, 대학원 에너지시스템학과 성기혁(박사과정) 학생과 채주형(석박통합과정) 학생이 공동저자로 참여했다.전 세계의 플라스틱 사용량은 매년 증가해, 2025년에는 445Mt(40만5000kg)의 플라스틱 생산이 예상되고 있다. 실생활에서 사용되는 플라스틱 중 저밀도 폴리에틸렌(LDPE, Low-Density Polyethylene)은 HDPE, PP, PS, PVC와 더불어 5대 범용 폴리머에 속하며 포장용 필름, 각종 일회용 용기 등 다양한 제품의 소재로 사용된다. 하지만 저밀도 폴리에틸렌(LDPE)의 원료인 에틸렌은 석유의 정제를 통해 생산되며, 전 세계적으로 플라스틱의 재활용률은 9%에 불과하다. 때문에 추가적인 탄소 배출을 막기 위해 이산화탄소(CO2)가 활용된 고분자의 생산이 요구되어 왔다.장혜영 교수팀은 앞선 연구에서 개발한 아연-갈산 박막 촉매를 활용해, 지구온난화의 주요 원인으로 꼽히는 이산화탄소(CO2)와 생분해성 플라스틱인 PLA(Polylactic acid)의 전구체로 사용되는 락타이드를 공중합하여 높은 촉매활성으로 고분자를 합성했다.또한 중합 방법에 따라 PLA의 비율을 9.4~76 wt%로 자유롭게 조절할 수 있는 기술을 개발하는 데에도 성공했다. 합성된 고분자는 기존에 널리 활용되던 저밀도 폴리에틸렌(LDPE)보다 더 높은 기계적 물성을 보여 이산화탄소 기반의 고분자가 기존의 석유 기반 플라스틱을 대체할 수 있는 가능성을 보여줬다.연구를 주도한 장혜영 교수는 “이번 연구는 기후온난화 가스로 알려진 이산화탄소를 활용한 고분자의 상용화를 앞당길 수 있다는 점에서 의미있는 결과”라고 밝혔다.이번 연구는 교육부의 G-LAMP 사업∙자율중점연구소사업과 한국연구재단의 중견연구자 지원사업의 지원을 받아 수행됐다.아주대 화학과 연구팀은 대표적 온실가스인 이산화탄소를 활용해 플라스틱을 생산할 수 있는 방법을 연구하고 있다
-
209
- 작성자통합 관리자
- 작성일2025-06-12
- 1590
- 동영상동영상
-
- 약물 방출 시간과 위치 정밀하게 설계·구현- <Bioconjugate Chemistry> 5월 온라인판 표지논문(Front Cover) 선정아주대 첨단바이오융합대학 연구팀이 생체 환경에서 약물의 방출 시간과 위치를 정밀하게 제어할 수 있는 기술을 개발했다. 이에 앞으로 정밀 약물 전달 기술 및 바이오이미징 등에 활용될 것으로 기대된다. 첨단바이오융합대학·대학원 분자과학기술학과 소속 김은하·김욱·유태현 교수 공동 연구팀은 ‘비스하이드록시 트랜스-사이클로옥텐(C2TCO)’이라는 생체적합성 링커 화합물을 간단하고 효율적으로 합성하는 기술을 개발했다고 밝혔다.해당 연구는 ‘다중 면역형광 이미징을 위한 생체정밀 클릭-투-릴리즈 시약 C2TCO의 간편한 합성과 응용(An easy access to bioorthogonal click-to-release reagent bishydroxy-trans-cycloocten(C2TCO) and harnessed its rapid labeling and dissecting feature in multicycle imaging)’이라는 제목으로 저명 학술지 <바이오컨쥬게이트 케미스트리(Bioconjugate Chemistry)> 5월 온라인판 표지논문(Front Cover)으로 선정됐다.아주대 대학원 분자과학기술학과의 박사후연구원 V. 아룬(Arun) 박사와 석박사 통합과정의 이민주·최홍서·이상우 학생이 공동 제1저자로 참여했고, 첨단바이오융합대학·대학원 분자과학기술학과의 김은하·김욱·유태현 교수가 교신저자로 함께 했다. 최준원 교수(첨단바이오융합대학·대학원 분자과학기술학과)는 공저자로 참여했다.이번 연구 성과는 최근 생물직교성 클릭 화학(Bioorthogonal Chemistry) 분야에서 전 세계적으로 주목받고 있는 ‘클릭-투-릴리즈(click-to-release)’ 반응 기술의 획기적 진전을 의미한다. 생물직교성 클릭 화학은 우리 몸속에서 일어나는 복잡한 화학 반응들과는 무관하게 설계자가 원하는 반응만을 일으킬 수 있는 ‘똑똑한 화학 기술’이다. 이 기술은 우리 몸의 단백질이나 DNA처럼 중요하고 다양한 생체 분자들과는 부딪히지 않고, 꼭 정해진 두 물질끼리만 빠르고 정확하게 결합할 수 있도록 도와주는데, 이를 ‘생물직교성’이라 한다. 이는 마치 자동차 안에서 누구나 안전벨트를 쉽게 결합(클릭)시킬 수 있는 것처럼, 비교적 손쉽게 정해진 물질끼리의 반응이 일어날 수 있도록 도와준다는 점에서 매우 유용하다. 지난 2022년 노벨화학상의 영예도 이 분야 연구자들에게 돌아간 바 있다. 그중에서도 ‘클릭-투-릴리즈’(click-to-release)라는 생물직교성 클릭 화학 기술을 사용하면, 설계자가 원하는 반응을 통해 약물이나 형광물질 같은 특정 물질을 원하는 시점과 장소에 ‘톡’ 떨어뜨려 방출할 수 있다. 이러한 기술을 활용하면 복잡한 절차 없이 몸속에서 원하는 곳에만 정확하게 약을 전달하거나 특정 반응을 일으킬 수 있다. 항체에 약물을 달아 주사하고, 이 약물이 암 조직 주변에 도달했을 때 다른 약물을 복약, 두 물질이 반응을 일으키며 활성화되도록 설계할 수 있는 것. 이에 최근에는 신약 개발에도 해당 기술이 널리 활용되고 있다. 아주대 연구팀은 기존의 클릭-투-릴리즈 시스템을 더욱 단순하고 효율적인 방식으로 구현해냈다. 클릭-투-릴리즈 반응에 활용되어 온 트랜스-사이클로옥텐(TCO)의 개량형인 생체적합성 링커 화합물 비스하이드록시 트랜스-사이클로옥텐(C2TCO)을 간단하면서도 안정적인 방식으로 합성하는데 성공한 것. 이를 통해 짧은 시간 안에 간단하게 합성이 가능하도록 공정을 효율화할 수 있었다. 연구팀은 이 기술을 적용해 형광체가 부착된 항체(C2TCO-FL)를 만들고, 이후 유기 화합물 테트라진을 이용해 형광 신호를 원하는 시점에 제거하는 데 성공했다. 이를 통해 하나의 세포 샘플을 반복적으로 다양한 항체로 염색·신호 제거·재염색하는 ‘다중 사이클 면역형광이미징’이 가능함을 입증해냈다. 바이오이미징 기술인 다중 사이클 면역형광이미징은 하나의 조직에서 수십 가지 단백질을 차례로 볼 수 있게 해주는 기술로, 질병을 더 정확히 분석할 수 있게 도와준다.아주대 연구진은 또한 암세포 표면 단백질 PD-L1을 표적하는 치료용 항체(아테졸리주맙)에 세포 독성 약물(MMAE)을 연결한 항체-약물 접합체(ADC)를 개발했다. 이 접합체는 테트라진 처리 시 표적 부위에서만 약물을 정밀하게 방출할 수 있어, 부작용을 줄이고 약효를 극대화할 수 있는 장점이 있다. 연구팀이 수행한 실제 세포 실험에서 실제 약물 방출 후 강력한 암세포 사멸 효과를 보였다.첨단바이오융합대학·대학원 분자과학기술학과의 김은하·김욱·유태현·최준원 교수(윗줄)와 대학원 분자과학기술학과의 박사후연구원 V. 아룬(Arun) 박사, 석박사 통합과정의 이민주·최홍서·이상우 학생(아랫줄)이번 연구를 주도한 김은하 교수는 “이번 연구는 클릭-투-릴리즈 시스템을 이용한 생체환경에서의 항체-페이로드 접합체 활성 정밀 제어 기술의 실용화를 위한 첫걸음”이라며 “현재 기초연구 단계로 앞으로 관련 연구의 확장을 통해 암 치료, 정밀 진단 등 다양한 분야에 활용될 수 있을 것”이라고 말했다.김은하 교수는 “앞으로 비스하이드록시 트랜스-사이클로옥텐(C2TCO)을 활용한 다양한 생체분해형 화합물 개발과 함께, 항체 외에도 다양한 전달체에 적용할 수 있는 후속 연구를 진행할 계획”이라고 덧붙였다. 한편 아주대 김은하·유태현·김욱 교수팀은 삼성미래기술육성사업의 지원을 받아 ‘STRIC 기술: 항체-페이로드 복합체 기반 면역항암제의 시공간적 활성 제어’를 주제로 공동 연구를 수행하고 있다. 연구팀은 클릭 화학을 접목한 생물직교성 반응을 활용해 생체 내 다른 유기물이나 생체고분자와의 비선택적인 상호작용 없이 항체-페이로드 접합체의 활성을 시공간적으로 조절할 수 있는 기술을 개발 중이다. 이를 통해 기존 항체-페이로드 접합체 기반 면역항암제가 지닌 한계를 극복하고자 하며, 이번에 개발한 기술 역시 해당 연구의 일환으로 관련 후속 연구도 활발히 이어지고 있다.이번 연구는 삼성미래기술육성사업, 글로벌기초연구실 사업, 중견연구자사업(연계 신진후속연구), 바이오의료기술개발 사업, 경기도 지역협력연구센터(GRRC), 아주대학교 교내연구비 사업의 지원을 통해 수행됐다. * 상단 이미지 : 아주대 연구팀의 연구 내용이 실린 <바이오컨쥬게이트 케미스트리(Bioconjugate Chemistry)> 5월 온라인판 표지_제공 ACS Publications
-
207
- 작성자통합 관리자
- 작성일2025-06-10
- 1470
- 동영상동영상
-
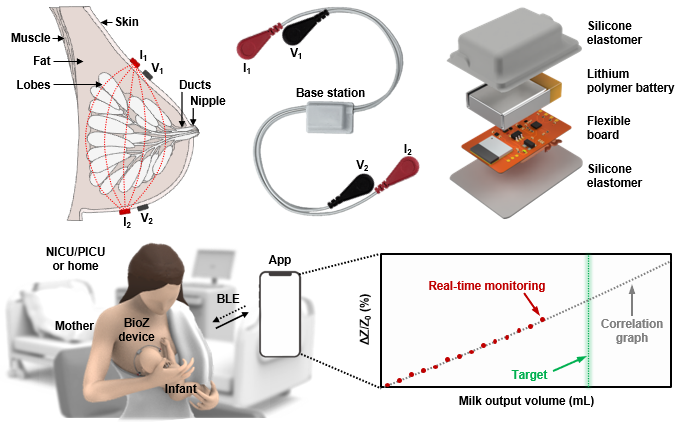
아주대 첨단바이오융합대학 김지혜 교수가 참여한 연구팀이 모유 수유 중에 영아의 모유 섭취량을 실시간 모니터링할 수 있는 무선 웨어러블 센서를 개발했다. 해당 연구는 ‘모유 수유 중 모유 섭취량의 실시간 모니터링을 위한 소형 무선 시스템(A compact, wireless system for continuous monitoring of breast milk expressed during breastfeeding)’이라는 제목의 논문으로 바이오메디컬 분야의 저명 학술지인 <네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)>에 5월 게재됐다. 김지혜 아주대 첨단바이오융합대학 교수(사진)가 제1저자로 참여했고, 오세용 한양대 전자공학부 교수와 라우델 아빌라(Raudel Avila) 미국 라이스대학 기계공학과 교수가 공동 제1저자로 함께 했다. 미국 노스웨스턴대(Northwestern University)·앤 앤드 로버트 H. 루리 시카고 아동병원(Ann & Robert H. Lurie Children‘s Hospital of Chicago)·성균관대 연구진도 이번 연구에 참여했다. 모유 수유는 영아의 건강과 발육을 위해 권장되어왔으나, 아이가 얼마나 모유를 섭취하는지를 파악하는 것은 그동안 부모와 의료진 모두에게 미지의 영역이었다. 지금까지는 수유 전후로 아기의 체중을 재는 방식 외에는 모유 섭취량을 측정할 방법이 없었던 것. 이러한 불확실성은 많은 산모들에게 불안과 자책감을 유발하고, 경우에 따라 모유 수유 포기로 이어지기도 한다. 이에 모유 수유량의 실시간 측정을 위해 연구팀은 다양한 방법을 시도했고, 근육량이나 지방량 등의 체성분 측정에 활용되는 생체 임피던스(Bioimpedance) 기술을 활용하는 방법을 고안해냈다. 이 기술을 활용하면 약한 교류 전류를 통과시켜 신체의 전기적 저항을 측정할 수 있다.연구팀은 유방에 두 개의 작은 패드를 붙여 약한 전류를 흘려보내고, 모유의 감소량에 따른 전압 변화를 읽어냈다. 또한 유방의 해부학적 구조를 컴퓨터로 시뮬레이션해, 수유 도중 일어나는 생리적 변화를 수치화했으며 센서의 위치에 따른 측정에의 영향을 분석해 기기를 고도화했다. 아주대 공동 연구팀이 개발한 모유 수유 중 영아의 모유 섭취량을 실시간으로 측정할 수 있는 무선 웨어러블 센서를 설명하는 그림 이미지 출처 <네이처 바이오메디컬 엔지니어링(Nature Biomedical Engineering)>이 기술을 활용하면 모유 섭취량을 스마트폰 어플리케이션을 통해 실시간 그래픽으로 시각화할 수 있다. 연구팀은 기술의 신뢰성·실용성을 ▲이론적 모델링 ▲유방 모사 모델 실험 ▲해부학 기반 유한요소법 시뮬레이션 등을 통해 검증했다. 더불어 실제 수유 중인 산모 12명을 대상으로 최대 17주간 병원 및 가정 환경에서의 임상실험을 진행했다. 이 센서 기술은 신생아의 영양 상태를 정밀하게 관리하고, 산모의 수유 불안감 해소에도 실질적으로 기여할 수 있을 것으로 기대된다. 연구팀은 이번 연구 개발 내용을 특허로 출원했고, 실제 생활에서의 활용과 발전을 위해 후속 연구를 진행할 계획이다. 김지혜 교수는 “이번에 개발된 센서로 모유수유와 관련한 불편함을 해소하고, 수유량에 대한 불확실성을 줄여 산모와 의료진 모두에게 신뢰할 수 있는 정보를 제공할 수 있게 됐다는 데에 그 의미가 있다”라고 설명했다.김 교수는 이어 “특히 신생아 중환자실 등 고위험 신생아의 영양 상태에 대한 임상적 관리를 개선하는 데 기여함으로써, 그동안 의료현장에서 해결되지 못했던 임상적 수요를 과학적으로 충족시킬 수 있는 사례가 될 것”이라고 덧붙였다.
-
205
- 작성자통합 관리자
- 작성일2025-05-29
- 1964
- 동영상동영상
-
아주대 연구진이 베타락탐(β-lactam) 항생제 내성균을 제어할 수 있는 새로운 유전자 표적을 규명하는데 성공했다. 이에 그동안 질병 치료 효과를 저해하는 주요 원인으로 꼽혀온 항생제 내성 문제의 해결에 중요한 역할을 할 수 있을 전망이다.연구 결과는 감염 미생물학 분야의 국제 저명 학술지 <이머징 마이크로브스 앤 인펙션스(Emerging Microbes & Infections)> 4월 온라인판에 ‘트랜스포존-시퀀싱 분석을 통한 플라스미드 유래 베타락탐 분해효소(β-lactamase) 보유 대장균의 베타락탐(β-lactam) 항생제 내성 조절 유전자 규명(Identification of Host Genetic Factors Modulating β-Lactam Resistance in Escherichia coli harboring plasmid-borne β-lactamase through Transposon-Sequencing)’이라는 제목으로 게재됐다. 해당 연구에는 아주대 이창한 교수(생명과학과, 위 사진 가운데)가 교신저자로, 김현희 연구교수(기초과학연구소, 위 사진 오른쪽)가 제1저자로, 석사과정 정정윤 학생(생명과학과, 위 사진 왼쪽)이 공동저자로 참여했다. 미국 미시간대학 하워드휴즈의학연구소(University of Michigan, Howard Hughes Medical Institute) 소속의 제임스 바드웰(James Bardwell) 교수도 공동저자로 함께 했다. 항생제는 세균 감염에 의한 질병을 치료하기 위해 널리 사용되는 약물이다. 특히 페니실린 같은 베타락탐(β-lactam) 계열의 항생제는 세균의 세포벽 합성을 저해하기 때문에, 다양한 감염 질환의 치료에 널리 사용되고 있다. 그러나 베타락탐 분해효소(β-lactamase)를 획득한 내성균의 확산으로 인해 베타락탐 계열 항생제의 치료 효과가 급격히 감소하는 문제가 발생해왔다. 특히 베타락탐 분해효소(β-lactamase) 유전자는 수평적 유전자 이동(horizontal gene transfer)을 통해 빠르게 퍼지며, 여러 종류의 항생제 계열에 내성을 갖게 되는 다제내성균 발생의 주요 원인 중 하나로 지목되고 있다. 이에 따라 항생제 내성은 전 세계적으로 ▲질병 치료 실패 ▲사망률 증가 ▲의료비 부담 가중 등 심각한 사회·경제적 문제를 초래하고 있다. 세계보건기구(WHO) 역시 인류 보건에 대한 주요 위협 중 하나로 항생제 내성 문제에 대해 경고해왔다.아주대 연구팀은 항생제 내성균의 규명과 제어를 위해 TEM-1 베타락탐 분해효소를 발현하는 대장균(Escherichia coli) 균주를 모델로 삼아 연구를 진행했다. 전장 유전체 수준의 돌연변이 분석 기법인 Tn-Seq(Transposon-Sequencing)를 적용해 베타락탐 내성에 관여하는 유전자를 체계적으로 탐색한 것. 그 결과 기존에 알려진 내성 관련 유전자 외에도 gshA, phoPQ, ypfN, skp 등 새로운 유전자들이 베타락탐 내성 조절에 중요한 역할을 한다는 사실을 새롭게 규명할 수 있었다. 특히 이들 유전자의 베타락탐 내성과 관련된 기능은 대장균에 국한되지 않고, 녹농균(Pseudomonas aeruginosa)과 살모넬라(Salmonella Typhimurium) 등 주요 병원성 세균에도 보존되어 있다는 사실을 확인했다.아주대 연구팀이 규명한 베타락탐(β-lactam) 분해효소 발현 대장균에서 베타락탐 내성 관련 유전자와 그 작용 기전을 나타낸 그림. 새롭게 발굴한 gshA, phoPQ, ypfN, skp 유전자가 세포막 및 세포막 단백질의 안정성 조절과 베타락탐 내성 관련 유전자 발현 조절을 통해 대장균의 베타락탐 내성에 기여하는 것으로 밝혀졌다이번 연구는 항생제 내성균의 생존 메커니즘을 분자 수준에서 정밀하게 이해하고, 이를 기반으로 새로운 치료 표적을 제시했다는 점에서 큰 의미를 가진다. 이창한 교수는 “항생제 내성은 과학적 주제를 넘어 인류의 생존과 직결된 시급하고 중대한 문제”라며 “이번 연구에서 발굴한 유전자들은 베타락탐 분해효소를 보유한 다제내성균을 효과적으로 제어하기 위한 신약의 개발에 중요한 기반이 될 것”이라고 밝혔다. 이어 “특히 세포막과 세포막 단백질의 안정성 유지 메커니즘을 표적으로 삼는 새로운 신약 개발 전략 수립에 기여할 수 있을 것으로 기대한다”라고 덧붙였다.이번 연구는 아주대학교가 수행하고 있는 대학기초연구소(G-LAMP) 사업, 자율운영중점연구소 지원사업, 기초연구실 지원사업, 중견연구자 지원사업의 지원을 받아 수행됐다.
-
203
- 작성자통합 관리자
- 작성일2025-05-29
- 1937
- 동영상동영상